孕期哪些药物是安全的?数据之匮乏令人触目惊心
本文来自微信公众号: 自然系列 ,作者:Nature Portfolio
出于安全考虑,药物临床试验一向都将孕妇排除在外。但现在这种情况开始有所转变。
在新冠疫情尤为严重的2021年,Kristin Wall怀上了第二个孩子。她的医生告诉她,对于新冠疫苗在孕妇中的安全性和有效性,人们所知甚少。观察性研究数据——来自那些不知道自己怀孕的情况下接种了疫苗的人——表明疫苗是安全的,所以她可以选择接种。尽管如此,她仍然需要自己权衡风险与获益。
Wall是美国埃默里大学的一名流行病学家,因此她在评估健康风险上比一般人强。但她的这一经历十分常见,绝非仅限于新冠疫情时。Wall说,人们常常不得不在信息有限或不完善的情况下为孕妇做出重要医疗决定。怀孕会对身体造成许多改变,其中包括药物在体内的代谢和分布方式。正因如此,一种药物在非怀孕者体内也许药效是可预测的,但在孕妇身上的作用变得大为不同。
目前来自大规模疫苗接种人群的可靠证据以及相继完成的临床试验均表明,基于信使RNA(mRNA)的新冠疫苗,以及其他诸如流感疫苗等不使用活病毒的疫苗,在孕期一般来说是安全有效的。其他一些药物在孕期的安全性也已明确:部分抗过敏药、抗抑郁药和抗生素被认为可在孕期安全使用。扑热息痛(即对乙酰氨基酚,泰诺的主要成分)也被认为是安全的孕期用药,尽管美国总统特朗普对此持反对意见。但目前也有其他一些药物已知存在孕期用药风险,例如在孕期服用抗癫痫药丙戊酸钠可能导致胎儿出现严重的发育障碍。
大多数人在孕期都会服用药物,部分统计数据表明在美国超过90%的孕妇有在孕期服药[1]。尽管如此,很多药物的安全性和有效性仍具有不确定性,这些药物包括部分止吐药、消炎药以及近十年内才获批的多数药物等,因为上述药物从未在孕妇身上进行过试验。人们担忧这样的试验可能引起不良后果,政策层面上对此亦存在限制,而这样就意味着孕妇基本上被排除于临床试验之外。因此,公共卫生官员和医务人员只能基于间接证据给出用药建议,这些间接证据包括动物研究、在非孕妇受试者中开展的临床试验以及药物上市后对服药孕妇所进行的观察性研究。
Wall表示“这方面有极大空白”。她和另一些人已经设计了一些临床试验,并成功在孕妇身上对埃博拉、HIV和部分妊娠期特定疾病的有关疗法进行了测试。他们既保障了受试孕妇及其胎儿的健康,又收集到了可靠数据。基于这些经验,他们开发了相关工具和指南,以帮助其他研究人员也能将孕妇纳入临床研究。尽管取得了这些进展,此类临床研究在执行、监管和伦理等层面依然存在障碍。
Wall表示,目前尚无证据表明特朗普时代的政策(例如名为“让美国再次健康”的社会运动)造成被纳入药物临床试验的孕妇出现数量上的减少。但她补充道,反对制药业的言论甚嚣尘上,可能会强化长期以来人们在孕期用药研究上的犹豫态度,进而妨碍当前为填补证据空白所做的种种努力。
在临床指南明确建议孕妇避免使用丙戊酸钠之前,Denise Astill曾在怀孕期间服用丙戊酸钠。对她而言,这方面的切实进展“关系到公平性”。她的一对双胞胎女儿在四岁时被诊出存在多种健康问题,包括认知障碍、听力障碍、肾功能损害、自闭症和注意缺陷多动障碍。
她的这段经历促使她在奥克兰创立了名为“新西兰胎儿抗惊厥药物综合征协会”的慈善组织,该组织为孕妇在怀孕期间服用抗癫痫药物提供指导。她表示,孕妇应该和其他人一样有机会获得依循证据的医疗服务。“当我们的医疗系统和医学研究都是立足于男性的,我们这些孕妇真的还能做出知情选择吗?”
沙利度胺的阴影
当下人们对在孕妇中开展研究所持有的谨慎态度,主要源于上世纪中叶的一场医学界灾难。20世纪50年代末,一种名为沙利度胺的药物在46个国家作为孕吐治疗药物上市,尽管它从未在孕妇身上被测试过。医生们很快发现,在孕期服用该药的母亲中,其所生婴儿出现肢体缺失或短缩现象的数量激增。
在多项研究证实了该药与超过10000名儿童的先天性障碍有关后,沙利度胺于20世纪60年代初被撤出市场。这场灾难重塑了药品监管制度,引出了最终将孕妇排除在外的更严格的测试标准。
1964年的《赫尔辛基宣言》规定了涉及人类的医学研究的伦理原则,其中孕妇被归类到了“脆弱群体”,与无法给出知情同意的人(如儿童或严重认知障碍者)同为一类。
美国药品监管机构在1977年不但禁止孕妇参与临床试验,甚至还禁止“具有生育潜力的女性”参与其中。尽管这项政策在20世纪80年代末和90年代初开始转变(当时美国国立卫生研究院要求女性需被纳入研究),但孕妇由于被视为脆弱群体,故而仍在上述研究中被边缘化。
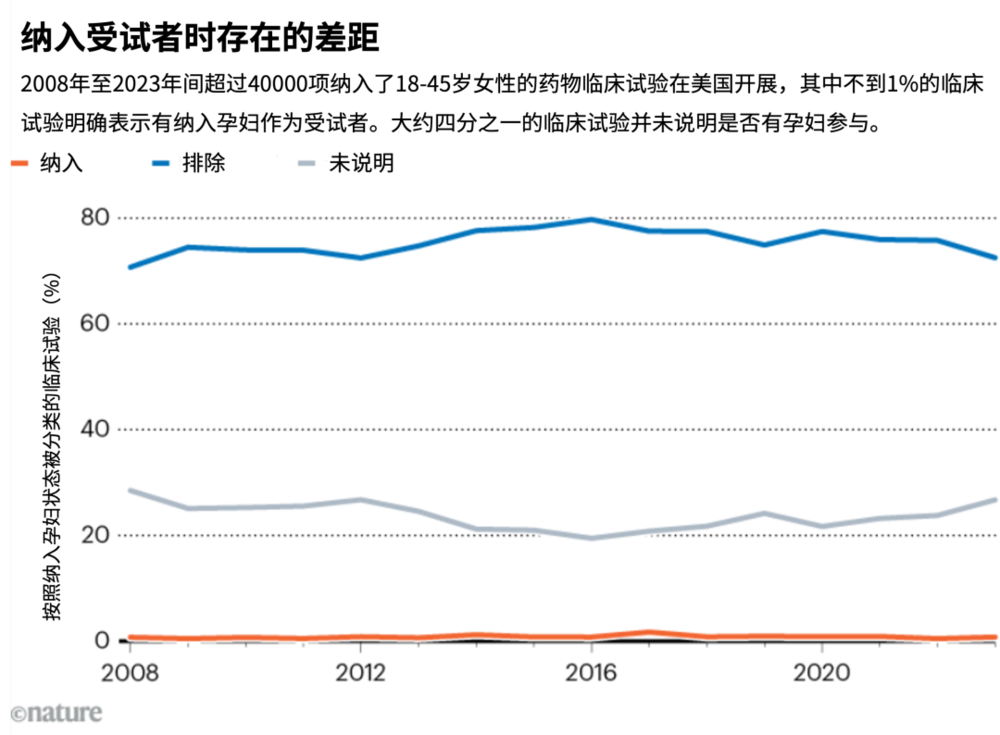
过去的十年中,部分上述限制已被放宽。世界卫生组织目前表示,孕妇应被视为“复杂”而非“脆弱”群体,并应在可能的情况下纳入试验。但相关进展仍然缓慢:一项对2008年至2023年间美国药物临床试验的分析发现,只有不到1%的试验明确说明纳入了孕妇作为受试者[2](见“纳入受试者时存在的差距”),而在欧盟国家提交的临床试验中这一比例还不到0.4%。

来源:参考文献2
一旦某一疗法获批,积攒相关证据可能需要耗费很长时间。就新冠疫苗而言,其接种人数众多,因此其证据积累迅速。到疫情结束时,大多数国家都已推荐孕妇接种该疫苗。但一项对获得美国食品药品监督管理局(FDA)批准的药物所进行的审查发现,如果一种药物在获批时其在孕期的安全性未知,那么平均需要27年才能有足够的证据来对其安全性进行较为可信的评价[3]。
美国布朗大学的统计学家Alyssa Bilinski说,这种证据上的空白让医生和孕妇面临艰难的选择:要么用风险不确定的药物治疗疾病,要么干脆不治。“有时候‘咨询你的医生’确实是个好主意,因为医生掌握了很多信息”,她说。“但‘咨询你的医生’也替代不了几十年来的研究不足”。
Bilinski的研究工作表明,将孕妇排除在随机对照试验之外可能是弊远大于利的做法。在她去年的一项研究中,她和同事评估了两类风险:一种是在孕妇身上测试药物,且其最终证明有害所带来的风险;另一种是完全不在孕妇身上测试该药物所带来的风险。他们的研究模型估计,如果沙利度胺在一个有200名孕妇参与的试验中进行过测试,大约会有33名儿童受到伤害[1];但这一试验本可以防止约8000例先天性障碍的发生,占1956年至1962年间所有沙利度胺相关病例的99.6%。
同一研究模型还表明,如果早期的新冠疫苗试验没有将孕妇排除在外,一些生命本可以得到挽救。当美国药品监管机构于2020年12月首次授权使用新冠疫苗时,尚无针对孕妇的具体数据。尽管孕妇在获取新冠疫苗上并未受限,但美国疾病控制与预防中心直到2021年8月才强烈推荐孕妇接种疫苗,而此时孕妇的新冠疫苗接种率已落后于一般人群。
该研究得出结论,如果当时有来自临床试验的针对孕妇的具体数据,由此带来的疫苗接种率提高和感染减少,本可以防止美国在2021年3月至11月期间约20%的新冠相关孕产妇死亡和死产发生,数量上总计超过200例。
许多人认为风险只来自于服用药物,但Bilinski认为不采取任何行动可能更加危险,因为这样会使孕妇及其婴儿暴露于未受控制的疾病或严重感染之下。“不进行试验的话,很可能导致集两者之短的最糟糕情况发生。”
打破障碍
伦敦大学学院的产科医生和母胎医学专家Anna David表示,将孕妇纳入临床试验时所面临的障碍,有些是真实存在的,有些则是人们观念上的。David认为,一个常见的误解是孕妇不会自愿参与。她的经验表明情况恰恰相反:当孕妇们获得与试验有关的尽可能多的信息时,她们是能够给予知情同意的,并且其中许多人愿意参与。
David认为另一个观念上的障碍是人们认为胎儿的健康状况在试验期间是无法被评估的,而这对于识别不良反应来说至关重要。“这完全是错误的,因为作为一名胎儿医学专家,我一直在做此类评估。”
为了使在纳入孕妇的临床试验中追踪和比较风险变得更容易,David及其同事们制定了标准化的概念定义和分级量表,用以评估可能影响孕妇和胎儿的问题,其中包括生长问题和积液等可通过胎儿影像检测到的问题[4]。David说,这些于2021年发布的举措已被纳入孕妇药物试验,并被数十篇论文引用,而且正在接受监管机构的验证。
她补充道,尽管有这些资源,但制药公司通常还是不愿意在孕妇身上对药物进行测试。其中的部分原因是他们担心不良结果会损害其声誉。“想象一下头条新闻上说‘某一新药会导致不良后果’,人们不想看到那种情况发生。”她说。
David认为另一个障碍是研究人员在获得保险时所面临的困难。在决定是否为临床试验承保时,保险公司通常依赖过往临床试验的数据来评估风险,包括先天性障碍等并发症。但是由于在孕妇人群中进行的试验很少,以至于几乎没有信息可用于指导这些评估。这种不确定性导致保险公司拒绝承保或要求收取高额保费。
即使保险能到位,在孕妇中开展的临床试验通常也比在其他人群中开展的试验更为昂贵,需要相关专业知识和基础设施。位于瑞士日内瓦的非营利组织“概念基金会”曾估计,与用于其他治疗领域的药物相比,开发一种专门用于孕期的药物可能需要额外花费570万美元,增加的成本主要来自安全性和有效性研究。
尽管存在这些障碍,目前还是已取得了一些进展。华盛顿大学西雅图分校的临床医生和科学家Sonali Kochhar说,来自数百万名接种了新冠疫苗的孕妇的真实世界数据,已帮助构建了强有力的安全性证据,并帮助转变了人们关于将这些孕妇纳入疫苗研究的观点。而且在过去几年中,还出现了两款专门为孕妇设计的疫苗。一种针对孕妇的呼吸道合胞病毒(RSV)疫苗于2023年在欧洲和美国获得批准。而另一种针对孕妇的B族链球菌(GBS)疫苗目前正在进行后期试验。在这两个案例中,孕妇通过胎盘传递给胎儿的抗体降低了生命早期发生严重感染的风险。
德国夏里特全球健康中心的疫苗学家Beate Kampmann说:“支持公司采用已充分考虑纳入孕妇的研究方案非常重要。”她领导了孕产妇RSV疫苗的后期临床试验,并提倡将孕妇纳入更多其它的疫苗试验中。“在发现有孕妇面临严重后果之前就应该开展相关研究,这可算一种伦理义务。”Kampmann说。
埃博拉和HIV的教训
一些疫苗研究会纳入孕妇,通常是因为对她们和孩子不作治疗的风险奇高。例如对感染者的婴儿几乎完全是致命的埃博拉,在该病暴发期间,卢旺达境内的一项研究在评估一种埃博拉疫苗的安全性和免疫反应时就有纳入孕妇,该疫苗先前仅获批用于非孕妇人群[5]。
在审查了来自200多名在孕中晚期入组的参与者的安全性数据后,一个外部组织批准了孕早期人员参与该研究,这些孕妇接受了额外的监测和更为频繁的检查。参与该试验的Wall说,由于孕早期出现流产或其他并发症的风险较高,人们通常对此时接种疫苗持谨慎态度。
社区的参与以及与当地卫生工作者的合作,帮助实现了所有孕期受试者中约95%的留存率。“对于超过2000名受试孕妇这样大的样本量来说,这是一个巨大的成功,这其中发挥了关键作用的是以研究参与者为中心的招募策略。”Julien Nyombayire说道,他是卢旺达家庭健康研究中心的一名临床医生,并开展了此项试验。
其他研究人员则正在运用类似原则来填补疾病治疗方面上的证据空白,包括目前缺乏有效治疗药物的妊娠期特定疾病。例如由南非斯泰伦博斯大学的临床科学家Cathy Cluver领导的一项国际合作研究,目前正在测试用于治疗子痫前期的药物。子痫前期是一种以高血压为特征的严重妊娠并发症。作为同类研究中规模数一数二的研究,该项目已对诸如传统糖尿病药物二甲双胍等进行试验,以便重新利用这些药物治疗子痫前期。得益于目前已有来自非孕妇人群的安全性数据,这种研究路径较易实施,Cluver说。
研究人员还对一种名为DM199的潜在药物进行测试,所纳入的受试者是因子痫前期和严重高血压入院、并计划引产的孕妇。该试验每次纳入一名受试者,并且从非常低的药物剂量开始测试,而后逐渐增加给药剂量。研究人员收集了母体血样和脐带血样,以评估药物是否能穿过胎盘,参与研究的护士会监测受试者的身体情况直至她们分娩,并在分娩后定期随访6周。
“事实上,能有个认识的人陪伴她们一起走过这段路程,这一点对受试者们来说意义重大,她们真的对此非常感激。”Cluver说。“这让我很震惊,应该我们说谢谢才是。”
英国利物浦大学的临床药理学家Catriona Waitt说,测试常规疾病用药的研究人员可以向妊娠期特定疾病用药的临床试验学习,还可以向HIV领域的研究学习。HIV的研究人员一直引领着当下在怀孕人群中所开展的高质量研究。她说,抗逆转录病毒药物可以保护母体健康、并阻断HIV病毒的母婴传播,其在妊娠中已开展的研究远超任何其他药物类别。
Waitt目前正在帮助世界卫生组织创建一个工具包,用以检测将用于怀孕人群的各种治疗方法。该工具包会囊括标准安全措施、即用型研究方案和以一致且高效的方式收集数据的工具。如此一来,HIV领域的研究经验就可以被应用到其他领域。
其他研究人员呼吁设立政府资助的基金,用以帮助覆盖潜在的保险索赔,并对该领域的研究加以鼓励。一些人提议,监管机构和资助者应鼓励研究人员们将孕妇纳入研究,比如要求研究人员证明其在参与者入组时排除孕妇的合理性,或提供激励措施,例如对于研究被忽视人群药物的开发者,为其提供加快审批的凭证。
伦敦健康研究慈善机构惠康基金会的生命伦理学家Carleigh Krubiner说,对研究的设计和监测给出明确指导,将有助于研究人员安全地进行研究,进而降低责任风险。
“目前存在大量错误信息,基于优良科学研究(获得)更多的证据,这将是我们通过研究来保护孕妇及其孩子所能做的最好的事。”Krubiner说。“我们需要努力将默认选择从‘排除’转变为‘纳入’。”
参考文献:
-
Bilinski,A.,Emanuel,N.&Ciaranello,A.Ann.Intern.Med.178,868–877(2025).
-
Bilinski,A.&Emanuel,N.Am.J.Obstet.Gynecol.232,e136–e139(2025).
-
Adam,M.P.,Polifka,J.E.&Friedman,J.M.Am.J.Med.Genet.C Semin.Med.Genet.157,175–182(2011).
-
Spencer,R.N.et al.Prenat.Diagn.42,15–26(2022).
-
Nyombayire,J.et al.Nature Med.31,3899–3906(2025).
-
Cluver,C.A.et al.BMJ374,n2103(2021).
原文以What drugs are safe during pregnancy?There’s a shocking lack of data标题发表在2026年2月11日《自然》的新闻特写版块上
©nature
Doi:10.1038/d41586-026-00331-3
#孕期哪些药物是安全的数据之匮乏令人触目惊心